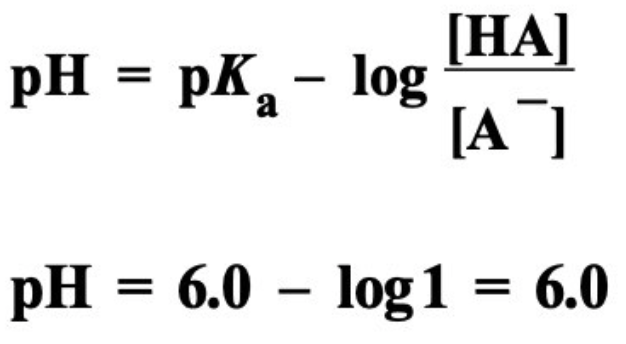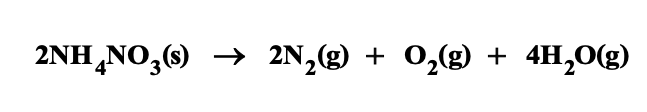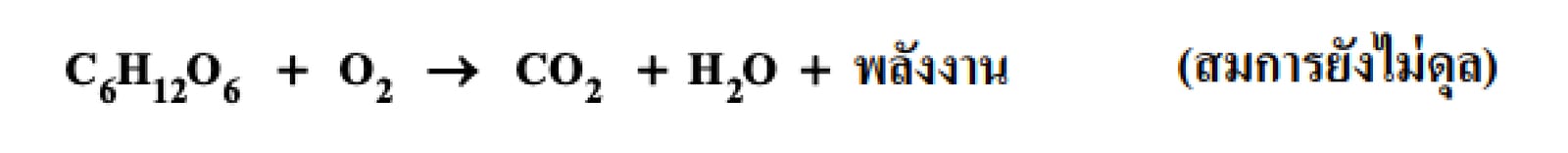วัดการประยุกต์ใช้ความรู้ซึ่งมีเนื้อหาตามสาระการเรียนรู้แกนกลางและสาระการเรียนรู้เพิ่มเติม
กลุ่มสาระการเรียนรู้วิทยาศาสตร์และเทคโนโลยี (ฉบับปรับปรุง พ.ศ. 2560) ตามหลักสูตรแกนกลางการศึกษาขั้นพื้นฐานพุทธศักราช
2551
ได้แก่ สาระที่ 2 วิทยาศาสตร์กายภาพ และสาระเคมี
โครงสร้างข้อสอบ
-
ข้อสอบ A-Level 65 Chem วิชาเคมี ประกอบด้วย 3 ส่วนคือ
- จำนวน: 15 - 17 ข้อ
-
ส่วนที่ 2 : สมการเคมีและการเปลี่ยนแปลงทางเคมี
1) ปริมาณสัมพันธ์
2) อัตราการเกิดปฏิกิริยาเคมี
3) สมดุลเคมี
4) กรด–เบส
5) เคมีไฟฟ้า
จำนวน: 15 - 17 ข้อ -
ส่วนที่ 3 : ทักษะในปฏิบัติการเคมีและการคำนวณปริมาณของสาร
1) ความปลอดภัยและทักษะในปฏิบัติการเคมี
2) โมล
3) สารละลาย
จำนวน: 2 - 4 ข้อ -
ประเภทข้อสอบ ปรนัย (5 ตัวเลือก) / ระบายคำตอบที่เป็นตัวเลข
ระยะเวลาที่ใช้สอบ 90 นาที
-
หมายเหตุ
1) ข้อสอบบางข้อมีการบูรณาการระหว่างเนื้อหา
2) ขอบเขตเนื้อหาของข้อสอบ สามารถศึกษาได้จาก เอกสารตัวชี้วัดและสาระการเรียนรู้แกนกลางกลุ่มสาระการเรียนรู้วิทยาศาสตร์ (ฉบับปรับปรุง พ.ศ. 2560) ตามหลักสูตรแกนกลางการศึกษาขั้นพื้นฐานพุทธศักราช 2551 จาก เว็บไซต์สำนักงานคณะกรรมการการศึกษาขั้นพื้นฐาน กระทรวงศึกษาธิการ
จำนวนข้อ
ตัวอย่างข้อสอบ
-
ตัวอย่างที่ 1 รูปแบบปรนัย 5 ตัวเลือก 1 คำตอบ
กำหนดพลังงานไอออไนเซชันลำดับที่ 1 ถึง 8 (ในหน่วยเมกะจูลต่อโมล) ของธาตุสมมติ 4 ธาตุที่มีเลขอะตอม
ไม่เกิน 20 ซึ่งอยู่ในคาบเดียวกัน ดังนี้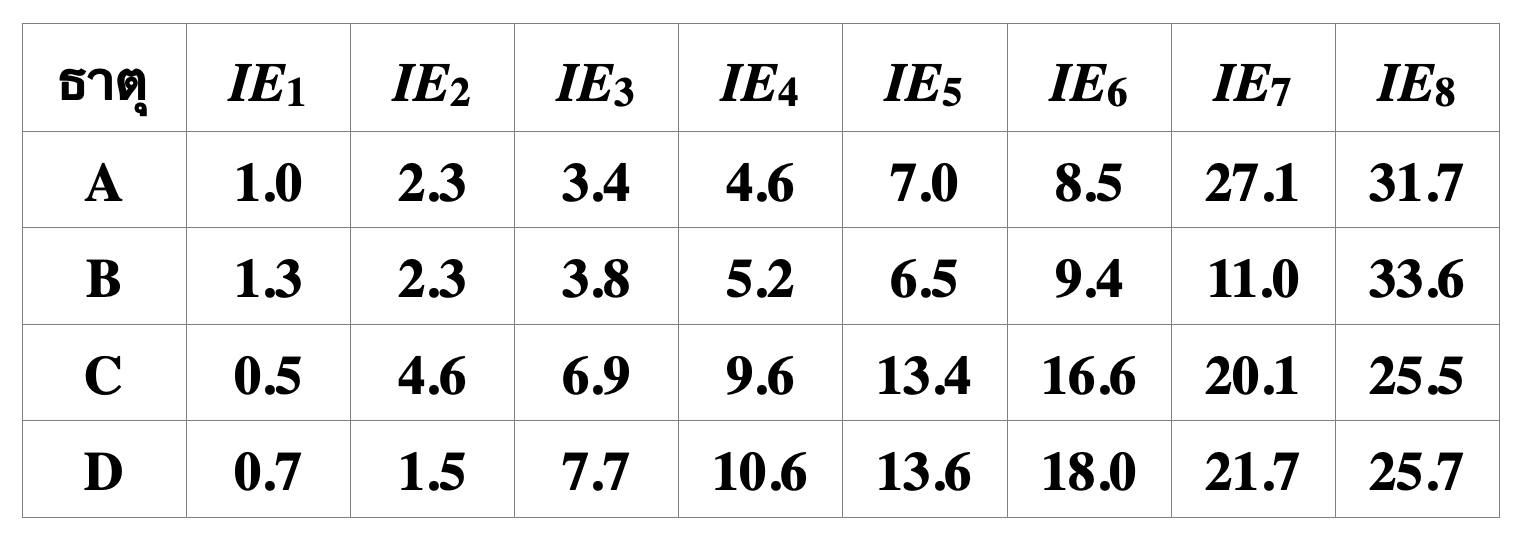
ข้อใดไม่ถูกต้อง
คำตอบ
เฉลย/เหตุผลและแนวคิดในการตอบคำถาม
จากพลังงานไอออไนเซชันลำดับต่าง ๆ ที่กำหนดให้ จะสามารถระบุหมู่ของธาตุได้ดังนี้
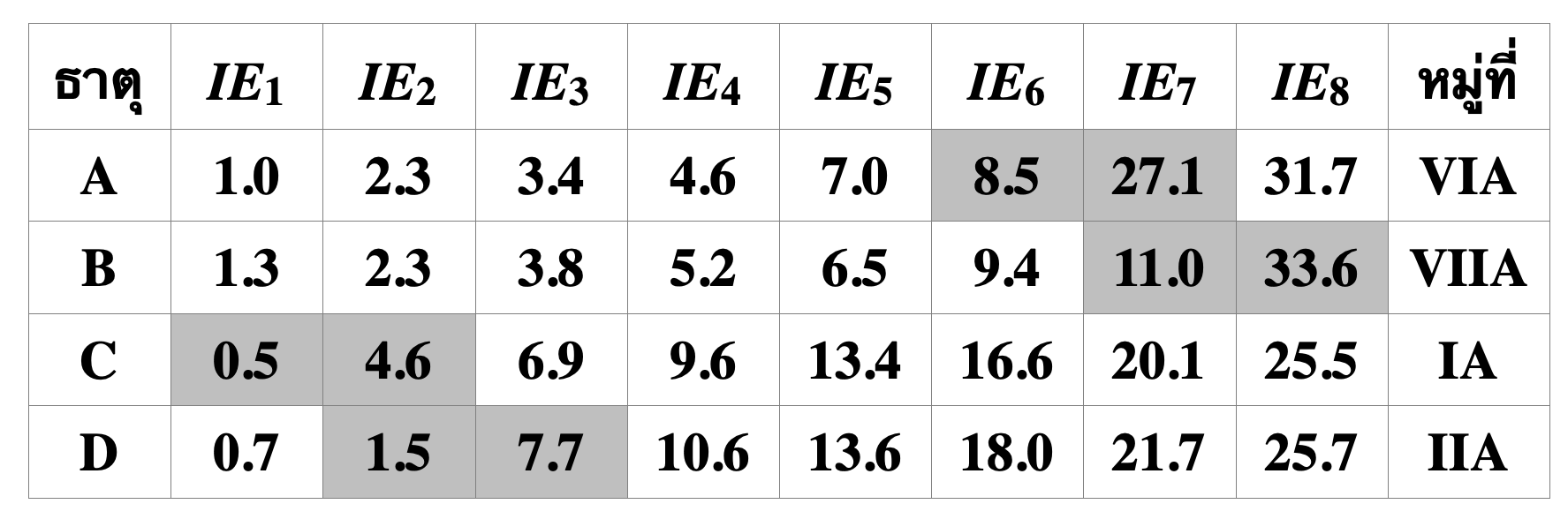
เมื่อพิจารณาหมู่ของธาตุทั้ง 4 ชนิดนี้ สามารถวิเคราะห์จำนวนอิเล็กตรอนและแนวโน้มสมบัติต่าง ๆ ได้ดังนี้
จำนวนอิเล็กตรอน : ธาตุทั้ง 4 ธาตุอยู่ในคาบเดียวกัน ซึ่งธาตุหมู่
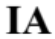 จะมีจำนวนเวเลนซ์อิเล็กตรอน
จะมีจำนวนเวเลนซ์อิเล็กตรอน
น้อยที่สุด ดังนั้น ธาตุหมู่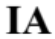 จึงมีจำนวนอิเล็กตรอนน้อยที่สุด ทำให้สามารถเรียงลำดับธาตุที่มีจำนวนอิเล็กตรอนจากน้อยไปมากได้ดังนี้
ธาตุ C < ธาตุ D <
ธาตุ A < ธาตุ B
จึงมีจำนวนอิเล็กตรอนน้อยที่สุด ทำให้สามารถเรียงลำดับธาตุที่มีจำนวนอิเล็กตรอนจากน้อยไปมากได้ดังนี้
ธาตุ C < ธาตุ D <
ธาตุ A < ธาตุ B ขนาดอะตอม : ธาตุทั้ง 4 ธาตุอยู่ในคาบเดียวกัน จึงมีเวเลนซ์อิเล็กตรอนอยู่ในระดับพลังงานเดียวกัน
แต่มีจำนวนโปรตรอนแตกต่างกัน ธาตุที่มีจำนวนโปรตรอนมากจะดึงดูดเวเลนซ์อิเล็กตรอนด้วยแรงที่มากกว่า ทำให้อะตอมมีขนาดเล็กกว่าธาตุที่มีจำนวนโปรตรอนน้อย โดยธาตุที่มีจำนวนโปรตรอนมากที่สุด คือ ธาตุ B รองลงมาคือ ธาตุ A ธาตุ D และธาตุ C ตามลำดับ ดังนั้น สามารถเรียงลำดับธาตุที่มีขนาดอะตอมจากขนาดเล็กไปใหญ่ ได้ดังนี้ธาตุ B < ธาตุ A < ธาตุ D < ธาตุ C
การนำไฟฟ้า : ธาตุ C อยู่ในหมู่
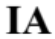 และธาตุ D อยู่ในหมู่
และธาตุ D อยู่ในหมู่ 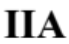 ซึ่งเป็นธาตุโลหะ จะนำไฟฟ้าได้ดีกว่าธาตุ A ซึ่งอยู่ในหมู่
ซึ่งเป็นธาตุโลหะ จะนำไฟฟ้าได้ดีกว่าธาตุ A ซึ่งอยู่ในหมู่ 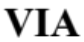 และธาตุ B ซึ่งอยู่ในหมู่
และธาตุ B ซึ่งอยู่ในหมู่ 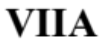 เนื่องจากเป็นธาตุอโลหะ
เนื่องจากเป็นธาตุอโลหะ
อิเล็กโทรเนกาติวิตี (
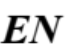 ) : ธาตุทั้ง 4 ธาตุอยู่ในคาบเดียวกัน
ความสามารถในการดึงดูดอิเล็กตรอนจะเพิ่มขึ้นจากหมู่
) : ธาตุทั้ง 4 ธาตุอยู่ในคาบเดียวกัน
ความสามารถในการดึงดูดอิเล็กตรอนจะเพิ่มขึ้นจากหมู่ 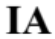 ไปหมู่
ไปหมู่ 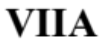 ดังนั้น สามารถเรียงลำดับธาตุที่มี
ดังนั้น สามารถเรียงลำดับธาตุที่มี 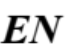 จากน้อยไปมาก ได้ดังนี้
จากน้อยไปมาก ได้ดังนี้
ธาตุ C < ธาตุ D < ธาตุ A < ธาตุ Bสัมพรรคภาพอิเล็กตรอน (
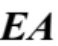 ) : ธาตุทั้ง 4 ธาตุอยู่ในคาบเดียวกัน ธาตุอโลหะมีค่า
) : ธาตุทั้ง 4 ธาตุอยู่ในคาบเดียวกัน ธาตุอโลหะมีค่า 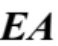 มากกว่าธาตุโลหะธาตุอโลหะจึงมีแนวโน้มที่จะรับอิเล็กตรอนได้ดีกว่าธาตุโลหะ โดยธาตุหมู่
มากกว่าธาตุโลหะธาตุอโลหะจึงมีแนวโน้มที่จะรับอิเล็กตรอนได้ดีกว่าธาตุโลหะ โดยธาตุหมู่ 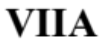 มีค่า
มีค่า 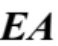 สูงที่สุด ดังนั้น สามารถเรียงลำดับธาตุที่มี
สูงที่สุด ดังนั้น สามารถเรียงลำดับธาตุที่มี 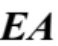 จากน้อยไปมาก ได้ดังนี้ธาตุ C <
ธาตุ D < ธาตุ A <
ธาตุ B
จากน้อยไปมาก ได้ดังนี้ธาตุ C <
ธาตุ D < ธาตุ A <
ธาตุ B ดังนั้น ข้อที่ไม่ถูกต้อง คือตัวเลือกที่ 4 ธาตุ C มี
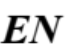 มากกว่าธาตุ D เนื่องจากธาตุ C มี
มากกว่าธาตุ D เนื่องจากธาตุ C มี 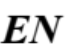 น้อยกว่าธาตุ D
น้อยกว่าธาตุ D -
ตัวอย่างที่ 2 รูปแบบปรนัย 5 ตัวเลือก 1 คำตอบ

พิจารณาข้อความต่อไปนี้
ก. จะละลายได้ดีขึ้นในสารละลายที่มีสมบัติเป็นกรด
จะละลายได้ดีขึ้นในสารละลายที่มีสมบัติเป็นกรด
ข. ปฏิกิริยาไปข้างหน้าของการเปลี่ยน เป็น
เป็น  เกิดได้ดี
เกิดได้ดี
ค. ละลายในน้ำได้ดีกว่า
ละลายในน้ำได้ดีกว่า 
ข้อความใดถูกต้อง
คำตอบ
เฉลย/เหตุผลและแนวคิดในการตอบคำถาม
ข้อความ ก. ในสารละลายที่มีสมบัติเป็นกรด
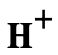 หรือ
หรือ 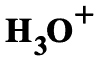 จะทำปฏิกิริยากับ
จะทำปฏิกิริยากับ 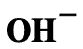 ทำให้ความเข้มข้น
ทำให้ความเข้มข้น
ของ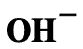 ลดลง ระบบจะปรับตัวไปในทิศทางที่เพิ่มความเข้มข้นของ
ลดลง ระบบจะปรับตัวไปในทิศทางที่เพิ่มความเข้มข้นของ 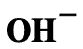 โดยเกิดปฏิกิริยาไป
โดยเกิดปฏิกิริยาไป
ข้างหน้าเพิ่มขึ้น ทำให้ ละลายได้ดีขึ้นในสารละลายที่มีสมบัติเป็นกรด ข้อความ ก. จึงถูกต้อง
ละลายได้ดีขึ้นในสารละลายที่มีสมบัติเป็นกรด ข้อความ ก. จึงถูกต้อง

ข้อความ ค. เมื่อพิจารณาสมดุลการละลายของ
 และ
และ  พบว่า ทั้งสองปฏิกิริยาเป็นการแตกตัว
พบว่า ทั้งสองปฏิกิริยาเป็นการแตกตัว
ของสารประกอบไอออนิกเป็นไอออน ซึ่งมีเลขสัมประสิทธิ์ทุกตัวเท่ากัน จึงสามารถพิจารณาความสามารถ
ในการละลายในน้ำได้จากการเปรียบเทียบค่า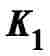 และ
และ 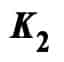 จะได้ว่า
จะได้ว่า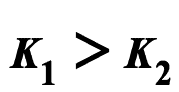 ดังนั้น
ดังนั้น  ละลายในน้ำได้ดีกว่า
ละลายในน้ำได้ดีกว่า 
ข้อความ ค. จึงไม่ถูกต้อง
ดังนั้น ข้อความที่ถูกต้อง คือ ก และ ข -
ตัวอย่างที่ 3 รูปแบบปรนัย 5 ตัวเลือก 1 คำตอบ
อินดิเคเตอร์ X และ Y มีช่วง pH การเปลี่ยนสีดังนี้

หยดอินดิเคเตอร์ทั้งสอง ชนิดละ 2 หยด ลงในสารละลาย HA 1.0 โมลาร์ ปริมาตร 100 มิลลิลิตร
เมื่อเติม NaOH 2.0 กรัม ลงในสารละลาย สารละลายจะเปลี่ยนจากสีใดเป็นสีใดกำหนดให้
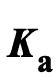 ของ
ของ 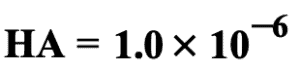
มวลต่อโมลของ NaOH เท่ากับ 40.0 กรัมต่อโมล
และอินดิเคเตอร์ทั้งสองชนิดไม่ทำปฏิกิริยากันคำตอบ
เฉลย/เหตุผลและแนวคิดในการตอบคำถาม
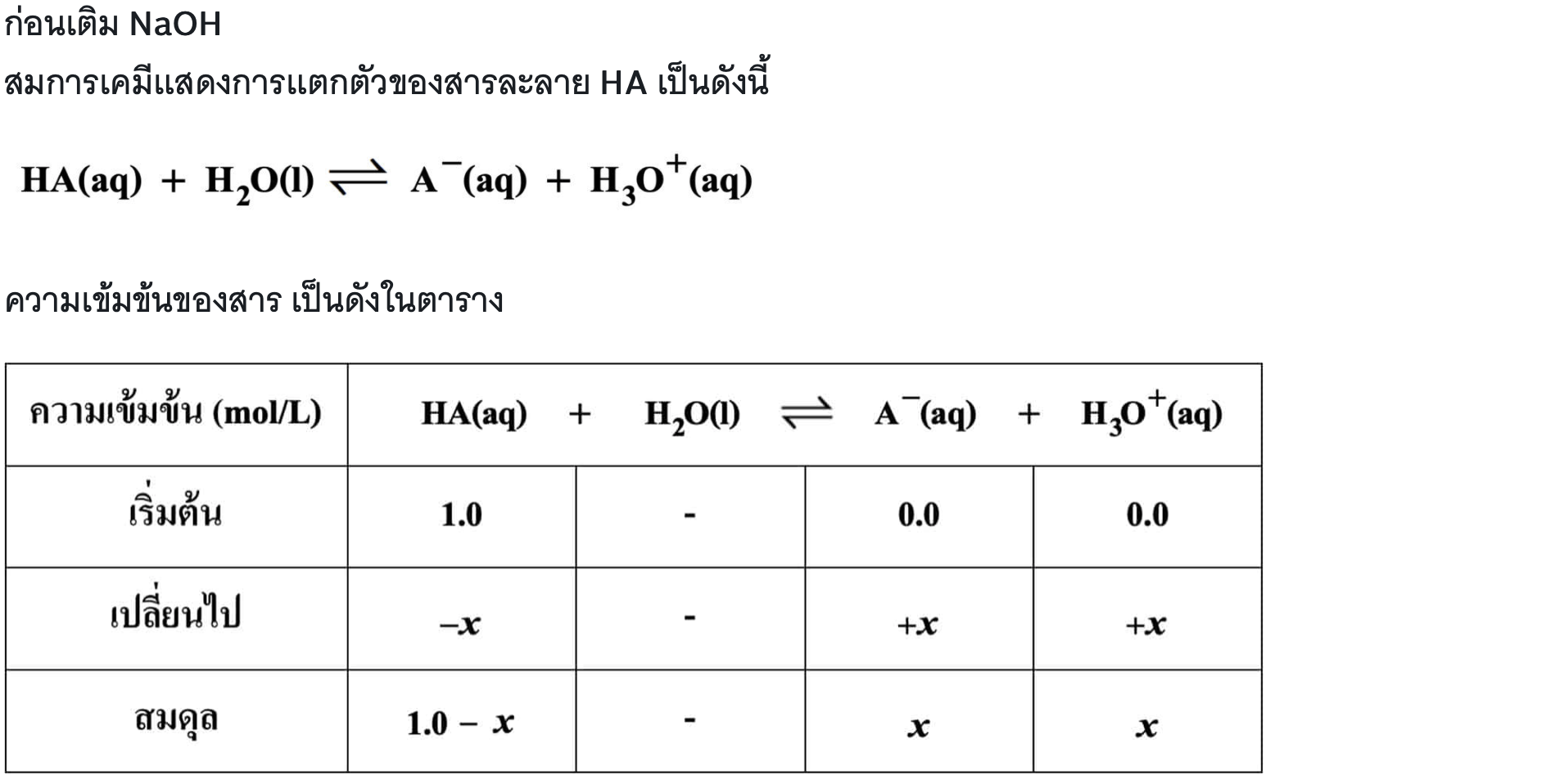


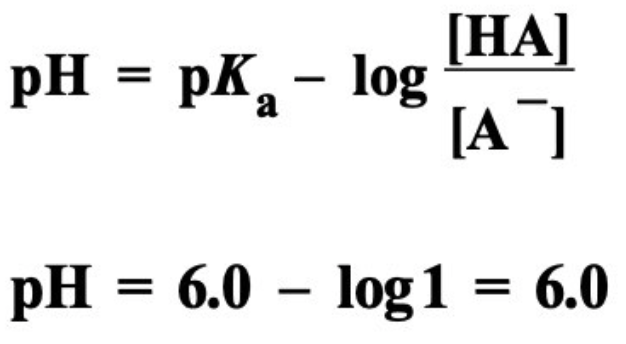
อินดิเคเตอร์ X จะมีสีน้ำเงิน และอินดิเคเตอร์ Y จะมีสีแดง จึงเห็นสารละลายเป็นสีม่วง
ดังนั้น เมื่อเติม NaOH 2.0 กรัม ลงในสารละลาย สารละลายจะเปลี่ยนจากสีส้มเป็นสีม่วง -
ตัวอย่างที่ 4 รูปแบบระบายคำตอบที่เป็นตัวเลข
แอมโมเนียมไนเทรตในรูปของแข็งจะเกิดการสลายตัว เมื่อได้รับความร้อนที่อุณหภูมิสูง ดังสมการเคมี
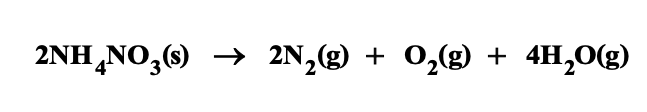
เมื่อแอมโมเนียมไนเทรต
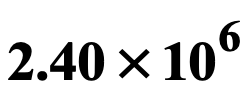 กิโลกรัมที่เก็บในโกดังขนาด 3,150 ลูกบาศก์เมตรสลายตัวทั้งหมด
กิโลกรัมที่เก็บในโกดังขนาด 3,150 ลูกบาศก์เมตรสลายตัวทั้งหมด
ที่อุณหภูมิ 3,000 เคลวินความดันของแก๊สทั้งหมดที่เกิดขึ้นในโกดังเท่ากับกี่เมกะปาสคาล

เฉลย/เหตุผลและแนวคิดในการตอบคำถาม
831 เมกะปาสคาล
คำอธิบาย

-
ตัวอย่างที่ 5 รูปแบบระบายคำตอบที่เป็นตัวเลข
แป้งชนิดหนึ่งมีสูตรโมเลกุลคือ
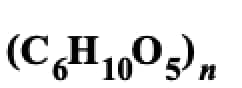 เมื่อเกิดปฏิกิริยาไฮโดรลิซิสอย่างสมบูรณ์จะได้ผลิตภัณฑ์เป็นกลูโคส
เมื่อเกิดปฏิกิริยาไฮโดรลิซิสอย่างสมบูรณ์จะได้ผลิตภัณฑ์เป็นกลูโคส 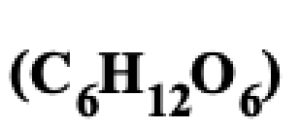
ดังสมการเคมี
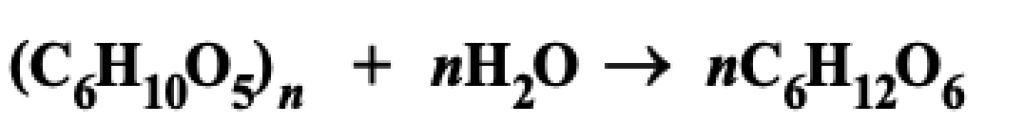
เมื่อร่างกายเผาผลาญกลูโคสจะให้พลังงาน ดังสมการเคมี
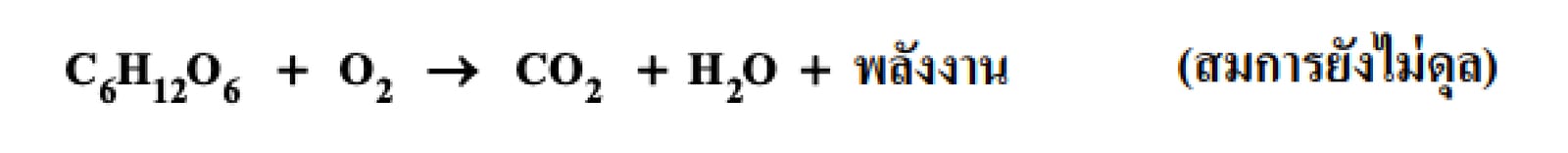
หากรับประทานอาหารชนิดหนึ่งปริมาณ 90.0 กรัม ซึ่งประกอบด้วยแป้ง 9.00% โดยมวล จะต้องใช้แก๊สออกซิเจน
อย่างน้อยกี่กรัมเพื่อเผาผลาญกลูโคสที่ได้จากแป้งในการรับประทานอาหารชนิดนี้ให้หมด
กำหนดให้ มวลต่อโมลของ H = 1.0 C = 12.0 และ O = 16.0 กรัมต่อโมลเฉลย/เหตุผลและแนวคิดในการตอบคำถาม
คำตอบที่ถูกคือ 9.60 กรัม


ดังนั้น หากรับประทานอาหารชนิดนี้ปริมาณ 90.0 กรัม จะต้องใช้แก๊สออกซิเจนอย่างน้อย 9.60 กรัม เพื่อเผาผลาญกลูโคสที่ได้จากแป้งในการรับประทานอาหารชนิดนี้ให้หมด